2021年12月31日,生物遗传股呼吁进行调查。最近,该公司的阿尔茨海默氏症药物,这是批准阿杜海姆作为食品药品监督管理局的负责人,下降了上周五。
在该药物于6月7日获得批准之前,美国食品和药物管理局代理专员珍妮特伍德库克博士要求监察长办公室调查美国机构和百健代表之间的互动。
伍德库克在周五发出的一封信中写道:“在我看来,监察长办公室等独立组织审查相关事件,以确定百健和FDA审查人员之间的任何互动是否与FDA的政策和程序不一致,这一点非常重要。
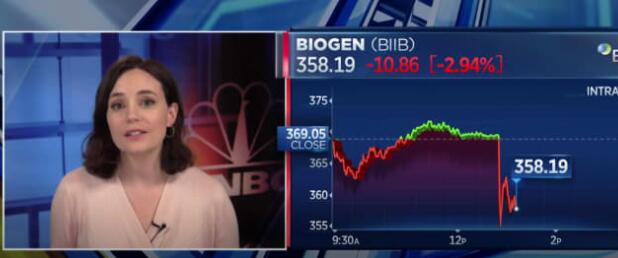
公告发布后,生物科技股价下跌超过3%。
在美国食品和药物管理局批准这家生物技术公司的药物后,生物基因的股票上个月飙升。这是美国监管机构批准的首个减缓阿尔茨海默病患者认知下降的药物,也是近20年来首个治疗这种疾病的新药。
这一决定标志着该机构独立外部专家组的建议偏离了该小组的建议,该小组去年秋天意外拒绝批准该药物,理由是数据不可信。在获得该机构的批准后,该组织至少有三名成员辞职以示抗议。
联邦监管机构面临着来自阿尔茨海默病患者朋友和家人的巨大压力。他们想快速追踪这种药物,科学上称为aducanumab。STAT News和其他媒体报道称,FDA官员利用监管捷径获得批准,以更快地将该药物推向市场。
Biogen的药物针对大脑中一种被称为淀粉样蛋白的“粘性”化合物,科学家预计这种化合物在破坏性疾病中发挥作用。
很少有食品和药物管理局官员要求调查该机构自己的决定。这是该公司和该药物的最新挫折,自2016年展示其前景以来,该药物一直备受争议。
2019年3月,在一个独立小组的分析显示该药物不太可能起作用后,Biogen停止了该药物的开发。几个月后,该公司宣布最终将寻求监管部门的批准,这让投资者感到震惊。
当Biogen在2019年底寻求该药物的批准时,其科学家表示,对更大数据集的新分析表明,aducanumab“减少了早期阿尔茨海默病患者的临床衰退”。
阿尔茨海默病专家和华尔街分析师立即表示怀疑。一些人怀疑临床试验数据是否足以证明药物有效,以及批准是否会使其他公司更难招募患者参与自己的药物试验。
一些医生表示,他们不会发行aducanumab,因为他们支持该公司应用的混合数据包。
标签:
